通过细胞类型特异性表达PD-L1和CTLA4Ig诱导异体细胞移植的局部免疫抑制
2023年12月12日,中国科学院动物研究所、北京干细胞与再生医学研究院胡宝洋、李伟、赵同标和吉林大学第一医院胡正共通讯在STEM CELL REPORTS期刊发表了题为“Induction of local immunosuppression in allogeneic cell transplantation by cell-type-specific expression of PD-L1 and CTLA4Ig”的文章,报道他们发现,利用伪装的干细胞衍生移植物或有望躲避宿主机体的免疫排斥反应。
研究人员对干细胞进行遗传工程化修饰以便从中获得的肝脏细胞对宿主机体的免疫系统不可见。与此同时,未成熟的潜在致瘤干细胞仍然会受到免疫系统的攻击和消灭,为了实现这一目的,这些细胞一旦转化为成熟的肝脏细胞,其就会产生两种免疫抑制性蛋白,而未成熟的干细胞则不会产生这些蛋白。
因此,当移植到携带人类免疫系统的小鼠机体中后,未成熟的干细胞就会被破坏,而肿瘤的形成也会受到抑制,而干细胞衍生的肝脏细胞则会被保护免于免疫攻击,尽管缺乏一定的免疫匹配,但其却能在小鼠体内持续存在。类似的方法还能被用来保护其它干细胞衍生的组织免受免疫排斥,比如心脏细胞或胰腺细胞等。目前这些干细胞衍生的移植物的安全性和有效性还需要在临床前和临床研究中进一步验证。
综上,本文研究中,研究人员阐明了一种强大且具有选择性的肝脏细胞特异性的免疫耐受诱导机制,从而就能改善移植物的存活率且不会出现可观察到的致瘤性;这种精准的免疫耐受策略或能帮助推进科学家们在再生医学研究中开发基于干细胞的治疗性策略。
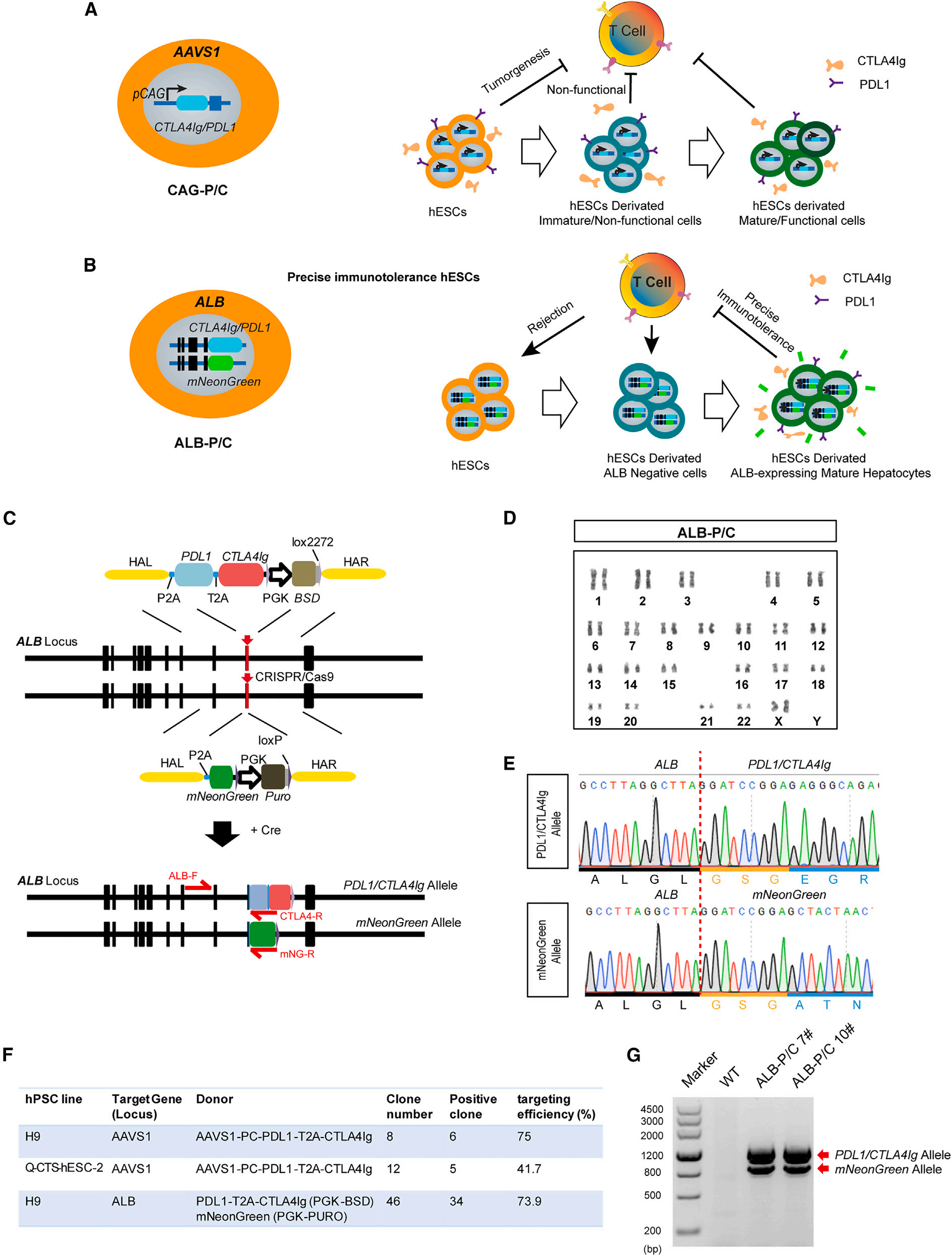
Figure 1. Generation and characterization of cell-type-specific immuno-tolerogenic hESC line, ALB-P/C hESCs
原文链接:https://doi.org/10.1016/j.stemcr.2023.10.016
